トファシチニブは、経口投与可能なヤヌスキナーゼ(JAK)の阻害剤であり、免疫調節作用と抗炎症作用があります。投与すると、トファシチニブはJAKに結合し、JAKシグナル伝達物質および転写活性化因子(STAT)シグナル伝達経路の活性化を防ぎます。これにより、インターロイキン(IL)-6、-7、-15、-21、インターフェロン-アルファおよび-ベータなどの炎症誘発性サイトカインの産生が減少し、炎症反応と炎症誘発性損傷の両方が予防される可能性があります特定の免疫疾患による。 JAKキナーゼは、造血、免疫、炎症に影響を与えるシグナル伝達経路に関与する細胞内酵素です。
トファシチニブは、中等度から重度の関節リウマチ、乾癬性関節炎、炎症性腸疾患の治療に使用されるヤヌスキナーゼの経口小分子阻害剤です。トファシチニブは、治療中の血清アミノトランスフェラーゼレベルの一時的で通常は軽度の上昇に関連していますが、臨床的に明らかな急性肝障害の症例にはまだ関連していません。
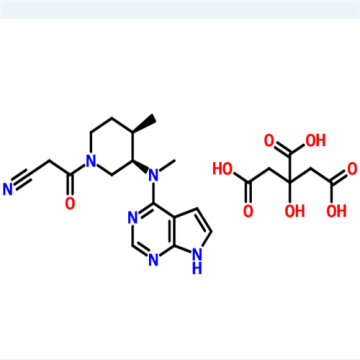
トファシチニブは、4位がN-メチル、N-(1-シアノアセチル-4-メチルピペリジン-3-イル)アミノ部分で置換されたピロロ[2,3-d]ピリミジンであるピロロピリミジンです。中等度から重度の活動性関節リウマチを治療するためのクエン酸塩として使用されます。 EC 2.7.10.2(非特異的プロテインチロシンキナーゼ)阻害剤および抗リウマチ薬としての役割を果たします。それはピロロピリミジン、N-アシルピペリジン、ニトリルおよび第三級アミノ化合物です。
クエン酸トファシチニブの化学系は3-{(3R、4R)-4-メチル-3- [メチル-(7H-ピロロ[2,3-d]ピリミジン-4-イル)-ピペリジン-1-イル]- 3-オキソ-プロピオニトリルクエン酸塩。ケミカルブックは、ファイザーが開発したヤヌスキナーゼ阻害剤です。 2012年11月6日、米国食品医薬品局(FDA)は、メトトレキサートに反応または耐性を示さない中等度から重度の活動性関節リウマチ(RA)の成人患者の治療薬としてこの物質を市場に出すことを承認しました。
トファチブは、メトトレキサートの有効性が不十分または耐えられない中等度から重度の活動性関節リウマチ(RA)の成人患者に適しています。メトトレキサートまたは他の非生物学的抗リウマチ薬(DMARD)と組み合わせて使用できます。
クエン酸トファチニブは、米国のファイザー製薬会社が開発した関節リウマチの治療薬です。メトトレキサートに対する反応が不十分または耐えられない中等度から重度の活動性関節リウマチ(RA)の成人に使用されます。この製品は、1日2回服用するヤヌスキナーゼ阻害剤です。 2012年11月6日、食品医薬品局(FDA)とファイザーは共同で、クエン酸トファチニブが、メトトレキサート治療に対して不十分または耐えられない反応を示した中等度から重度の活動性関節リウマチ(RA)の成人患者に承認されたことを発表しました。 Xeljanzは、単一の治療法として、またはメトトレキサートまたは他の非生物学的疾患緩和抗リウマチ薬(DMARD)と組み合わせて使用できます。この薬は、生物学的DMARDまたはアザチオプリンやシクロスポリンなどの強力な免疫抑制剤と組み合わせて使用しないでください。 xeljanzの承認された用量は1日2回、1回あたり5mgでした。 7つの臨床試験で、中等度から重度の活動性化学物質の成人を対象としたクエン酸トファチニブの安全性と有効性が評価されました。すべての試験において、xeljanzで治療された患者は、プラセボを投与された患者と比較して、臨床反応と身体機能に有意な改善が見られました。臨床試験では、最も一般的な副作用は上気道感染症、頭痛、下痢、鼻づまり、喉の痛み、鼻咽頭炎でした。 xeljanzの使用は、日和見感染、結核、癌、リンパ腫などの重篤な感染症のリスクの増加と関連しています。 xeljanz製品ラベルには、これらのセキュリティリスクに関するフレーム付きの警告が含まれています。 xeljanzの治療は、コレステロール値と肝酵素値の増加、および血球数の減少にも関連していました。心臓病、癌、重度の感染症に対するxeljanzの長期的影響を研究するために、FDAは、xeljanz(クエン酸トファシチニブ)治療の2用量を評価し、別の承認された治療を受けた対照群に含める市場後研究を要求しています。
私たちのトファシチニブAPIと中間体は次のとおりです。私たちは以下のすべてのAPIと中間体を一年中提供しています。
トファシチニブ中間Cas3680-69-1、トファシチニブAPI Cas 540737-29-9